ITP
ITP
Doptelet® ist zugelassen zur Behandlung von primärer chronischer Immunthrombozytopenie (ITP) bei erwachsenen Patienten, die auf andere Therapien
(z. B. Kortikosteroide, Immunglobuline) nicht ansprechen.1
Avatrombopag Wirkmechanismus
Dauer: 3:40 Min.
TPO-RAs: Bestehende Behandlungsoptionen sind oft kompromissbehaftet2-7
Ernährungs-
einschränkungen3,4
Unkorrekte Anwendung/
Mangelnde Compliance3,4
Hepatotoxizität/
Leber-Monitoring2
Subkutane
Anwendung2,5
Zeit die Spielregeln zu ändern!
Schnell
Zielwert bereits am 8. Tag erreicht8,*
Andauernd
Konstant im Zielbereich über 3 Monate8
* 65,6 % der Patienten auf/über Zielwert ≥ 50 x 109/L am 8. Tag.

Wirksamkeit – schnell und andauernd
Doptelet® zeigte bei ITP-Patienten in der Zulassungsstudie eine schnelle und andauernde Wirksamkeit (Zielwert-Erreichung von ≥ 50 x 109/L)8
Schneller Wirkeintritt
65,6 % der Patienten auf / über Zielwert ≥ 50 x 109 / L am 8. Tag8,*
Andauernde Wirksamkeit
Patienten bleiben über 3 Monate auf / über Zielwert ohne Notfall Medikation (median)8,*
* n = 32; Doptelet® vs. 0,0 unter Placebo (p < 0,0001).
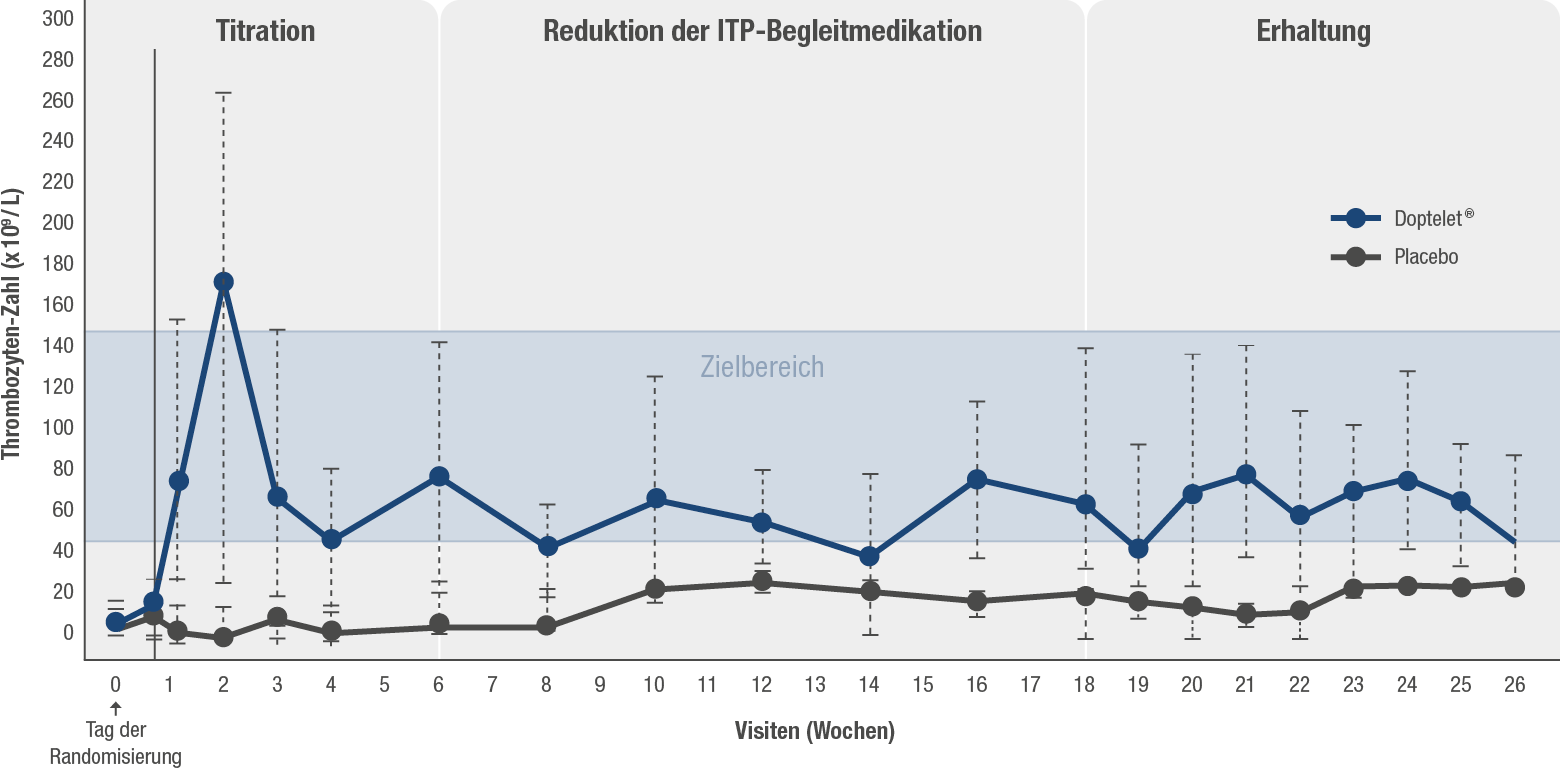
Doptelet®: Thrombozyten konstant im Zielbereich8
Mediane Thrombozyten-Zahl unter Doptelet®: 80,5 x 109/L vs. 8 x 109/L unter Placebo.11
Kumulative Anzahl der Wochen mit Thrombozytenansprechen (definiert als Thrombozytenwert ≥ 50 x 109/l) während der 6-monatigen Behandlung, ohne dass eine Notfalltherapie angewendet wurde. Avatrombopag erwies sich Placebo gegenüber als überlegen in der medianen kumulativen Anzahl der Wochen mit Thrombozytenansprechen (12,4 vs. 0,0 Wochen; p < 0,0001).

1 Tablette, 1x täglich1
Kein Lebermonitoring notwendig1
Doptelet® bei chronischer Immunthrombozytopenie:1
- Startdosis 20 mg 1 x täglich zusammen mit einer Mahlzeit
- Falls erforderlich Dosisanpassung in 20 mg-Schritten auf Basis des Thrombozytenwertes
- Eine Tagesdosis von 40 mg sollte nicht überschritten werden
Dosierung

Verträglichkeit
Unter Studienmedikation aufgetretene UEs Gesamt1,8
Doptelet® 4,3 % vs. 6,6 % Placebo
Schwerwiegende UEs Gesamt1,8
Doptelet® 1,2 % vs. 0,7 % Placebo
Expositionsbereinigte Inzidenzrate von Nebenwirkungen (%)1,8,#
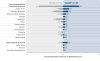
# Expositionsbereinigte Inzidenzrate von Nebenwirkungen (= Anzahl der Ereignisse geteilt durch die Gesamtzahl der Patientenwochen mit Exposition x 100) ist aufgrund der hohen Abbruchrate von Placebo-behandelten Patienten (16 von 17) während der Kernstudie und der dadurch kürzeren Behandlungsdauer dieser Patienten aussagekräftiger als eine nichtbereinigte Darstellung.
▼ Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung
TPO RA: Thrombopoetin Rezeptor Agonist; UEs: unerwünschte Ereignisse.
-
Aktuelle Fachinformation Doptelet®.
-
Al-Samkari H und Kuter DJ. Immune thrombocytopenia in adults: Modern approaches to diagnosis and treatment. Semin Thromb Hemost. 2020; 46(3): 275 – 288.
-
Cheloff AZ und Al-Samkari H. Avatrombopag for the treatment of immune thrombocytopenia and thrombocytopenia of chronic liver disease. J Blood Med. 2019; 10: 313 – 321.
-
Cantoni S et al. Alternate use of thrombopoietin receptor agonists in adult primary immune thrombocytopenia patients: A retrospective collaborative survey from Italian hematology centers. Am J Hematol. 2018; 93(1): 58 – 64.
-
Jin J et al. Factors affecting therapeutic compliance: A review from the patient’s perspective. Ther Clin Risk Manag. 2008; 4(1): 269 – 286.
-
Provan D et al. Updated international consensus report on the investigation and management of primary immune thrombocytopenia. Blood Adv. 2019; 3(22): 3780 – 3817.
-
Neunert CE et al. American Society of Hematology 2019 guidelines for immune thrombocytopenia. Blood Adv. 2019; 3(23): 3829 – 3866.
-
Jurczak W et al. Phase 3 randomised study of avatrombopag, a novel thrombopoietin receptor agonist for the treatment of chronic immune thrombocytopenia. Br J Haematol. 2018; 183(3): 479 – 490.